1.1. Primary battery ( 일차전지 ) vs. Secondary battery ( 이차전지 )
일차전지는 한 번 방전되면 다시 원래대로 충전할 수 없어
재사용이 불가능한 전지이다.
우리가 흔히 쓰는 일회용 건전지, 이런 것들은
일차전지라고 할 수 있다.
이차전지는 방전되어도 다시 전기를 이용하여
원래대로 충전할 수 있어
여러 번 재사용이 가능한 전지이다.
재사용이 가능한 전지나 무한대로 사용가능한 것은 아니다.
이차전지는 충방전을 반복하기 때문에
충전, 방전을 모두 알아야 설명이 가능하다.
따라서 이에 대해 설명하려고 한다.
1.2. Discharging ( 방전 )
Discharging, 방전에 대해 설명하자면
방전 과정은 Galvanic cell ( 갈바니 전지 ) 와 같다고 할 수 있다.
Galvanic cell은
전기화학적 ( chemical ) 에너지를
전기적 ( electrical ) 에너지로 전환하는 cell로
gibbs energy 변화량이 양수로 자발적이며
전자는 - 전극에서 + 전극으로 이동한다.
※ - 전극은 낮은 전위를 가지는 전극 ( 높은 electron E ),
+ 전극은 높은 전위를 가지는 전극 ( 낮은 electron E )
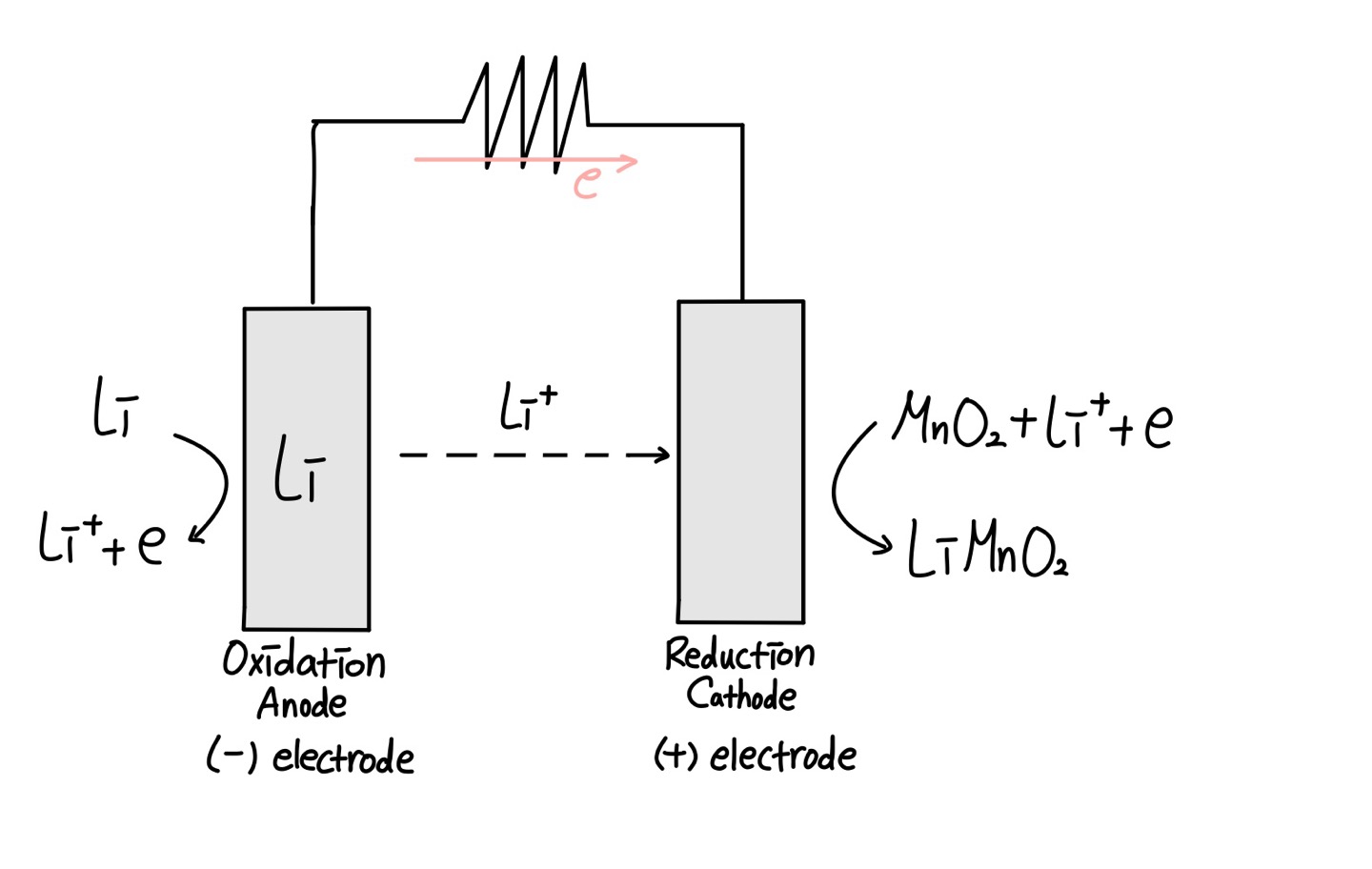
따라서 방전 과정은 위의 그림처럼 일어나며
Galvanic cell과 비슷한 양상을 보인다.
- 전극에서 + 전극으로 전자가 이동하고
자발적인 과정이며
- 전극에서 산화반응, + 전극에서 환원반응이 일어난다.
※ cathode는 전류가 흘러 나오는 곳,
anode는 전류가 흘러 들어가는 곳
1.3. Charging ( 충전 )
Charging, 충전에 대해 설명하자면
방전 과정은 Electrolytic cell ( 전해 전지 ) 와 같다고 할 수 있다.
Electrolytic cell은
전기적 ( electrical ) 에너지를
전기화학적 ( chemical ) 에너지로 전환하는 cell로
gibbs energy 변화량이 음수로 비자발적이며
전자는 + 전극에서 - 전극으로 이동한다.
※ - 전극은 낮은 전위를 가지는 전극 ( 높은 electron E ),
+ 전극은 높은 전위를 가지는 전극 ( 낮은 electron E )
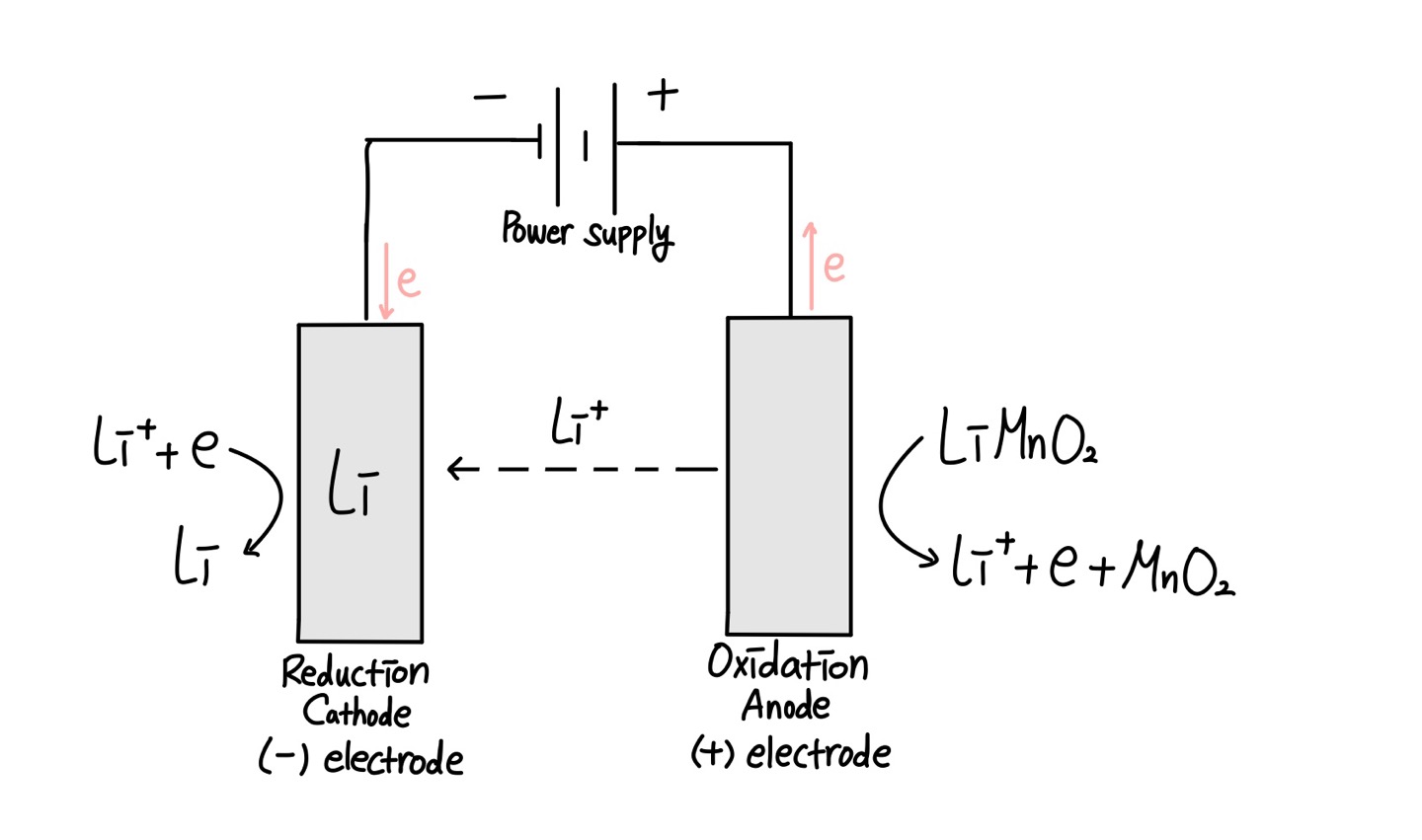
따라서 충전 과정은 위의 그림처럼 일어나며
Electrolytic cell과 비슷한 양상을 보인다.
+ 전극에서 - 전극으로 전자가 이동하고
비자발적인 과정이며
- 전극에서 환원반응, + 전극에서 산화반응이 일어난다.
※ cathode는 전류가 흘러 나오는 곳,
anode는 전류가 흘러 들어가는 곳